No se ha encontrado investigadores para este término.
Nuestro principal objetivo es desentrañar las vías moleculares a través de las cuales la dieta modula en salud y enfermedad. La dieta constituye la principal fuente de nutrientes, y existe una sólida evidencia de que tanto el tipo como la cantidad de alimentos que consumimos tienen un impacto importante en el riesgo y la progresión de múltiples enfermedades. Sin embargo, los mecanismos moleculares que subyacen a estos efectos siguen sin comprenderse completamente. Abordar esta cuestión es esencial para determinar cómo factores dietéticos concretos modulan vías de señalización biológica específicas que ejercen un impacto sobre la salud y la enfermedad.
Uno de los ejes centrales de nuestro trabajo es el estudio de la cetosis y de su impacto sobre la fisiología humana. La cetosis es un estado metabólico conservado desencadenado por la restricción de carbohidratos y caracterizado por un aumento de los niveles circulantes de cuerpos cetónicos, particularmente β-hidroxibutirato (BHB). Aunque tradicionalmente se ha considerado una fuente alternativa de energía en condiciones de escasez de glucosa, actualmente el BHB se reconoce como un metabolito señalizador con amplios efectos biológicos. A pesar del creciente interés en el uso de intervenciones basadas en cetosis en patologías como la obesidad, la diabetes, el cáncer, la inflamación y el envejecimiento, los mecanismos mediante los cuales el BHB y la cetosis tienen un efecto en la fisiología del organismo siguen estando pobremente definidos. Esta falta de comprensión mecanística, junto con resultados clínicos variables y en ocasiones contradictorios, limita su aplicación terapéutica segura y eficaz.
Nuestro trabajo reciente ha identificado una vía metabólica previamente no descrita en la que la enzima citosólica CNDP2 conjuga BHB con aminoácidos para formar una nueva clase de metabolitos: los BHB-aminoácidos. Estos metabolitos endógenos están presentes tanto en ratones como en humanos, y sus niveles circulantes son regulados dinámicamente por la cetosis. Hemos demostrado que los BHB-aminoácidos son metabolitos bioactivos capaces de suprimir el apetito en ratones, estableciendo así un vínculo mecanístico entre la cetosis y el control del peso corporal en obesidad.
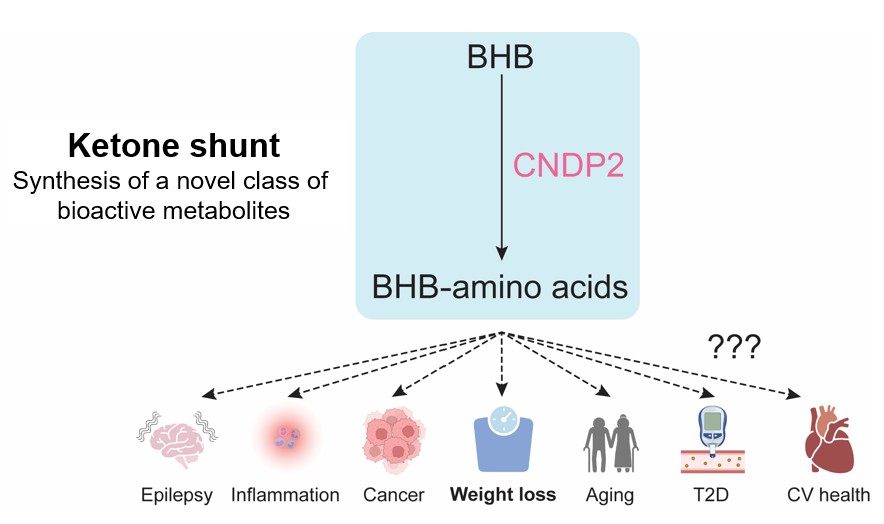
La identificación de esta vía de derivación cetónica (“ketone shunt pathway”) abre la posibilidad de revisitar cuestiones clásicas de la biología de los cuerpos cetónicos desde una nueva perspectiva, planteando qué otros mecanismos de la cetosis podrían haber pasado desapercibidos al no haber reconocido previamente estos metabolitos y su vía metabólica. El siguiente reto consiste en definir los contextos fisiológicos y patológicos en los que esta vía opera y evaluar su relevancia más allá de la obesidad.
Actualmente, nuestro trabajo se centra en comprender las funciones biológicas de estos metabolitos en contextos fisiológicos y patológicos en los que previamente se ha implicado a la cetosis o al BHB, particularmente en inflamación y cáncer. De manera más amplia, nuestro objetivo es investigar y desorfanizar vías metabólicas y metabolitos que median los efectos de la dieta sobre la salud humana.
Nuestra investigación se enmarca en el área de Medicina Personalizada y posee aplicaciones tanto terapéuticas como de descubrimiento de biomarcadores. Al mismo tiempo, contribuye al área de Genómica Funcional mediante el descubrimiento y la caracterización mecanística de nuevas vías metabólicas reguladas por la dieta implicadas en inflamación y cáncer.
Nuestras líneas de investigación:
Integramos bioquímica y metabolómica como herramientas de descubrimiento. Estos estudios se complementan con validación funcional en modelos celulares y animales, así como con estudios traslacionales en muestras humanas mediante colaboraciones clínicas.
Bibliografía relacionada con las líneas de investigación del grupo
Moya-Garzon, M. D.; Wang, M.; Li, V. L.; Lyu, X.; Wei, W.; Tung, A. S.-H.; Raun, S. H.; Zhao, M.; Coassolo, L.; Islam, H.; Oliveira, B.; Dai, Y.; Spaas, J.; Delgado-Gonzalez, A.; Donoso, K.; Alvarez-Buylla, A.; Franco-Montalban, F.; Letian, A.; Ward, C. P.; Liu, L.; Svensson, K. J.; Goldberg, E. L.; Gardner, C. D.; Little, J. P.; Banik, S. M.; Xu, Y.; Long, J. Z. A β-Hydroxybutyrate Shunt Pathway Generates Anti-Obesity Ketone Metabolites. Cell 2025, 188 (1), 175-186.e20. https://doi.org/10.1016/j.cell.2024.10.032.
Número de expediente: RYC2024-048926-I
IP: Dra. Maria Dolores Moya Garzon
Entidad financiadora: Ministerio de Ciencia, Innovación y Universidades (Agencia Estatal de Investigación)
Periodo de ejecución: 04/2026 – 03/2031









